- Pengarang Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:46.
- Diubah suai terakhir 2025-06-01 07:37.
Perbezaan utama antara nitrogen monoksida dan dinitrogen pentoksida ialah nitrogen monoksida ialah gas tidak berwarna manakala dinitrogen pentoksida ialah pepejal putih.
Nitrogen monoksida dan dinitrogen pentoksida ialah sebatian kimia yang mengandungi nitrogen dan oksigen. Ini adalah oksida nitrogen. Walau bagaimanapun, ia mempunyai sifat kimia dan fizikal yang berbeza.
Apakah itu Nitrogen Monoksida?
Nitrogen monoksida ialah sebatian tak organik yang mempunyai formula kimia NO. Kami memanggilnya nitrik oksida kerana ia adalah oksida nitrogen. Ia sebenarnya radikal bebas kerana ia mempunyai elektron yang tidak berpasangan. Selain itu, ia adalah molekul diatomik heteronuklear.
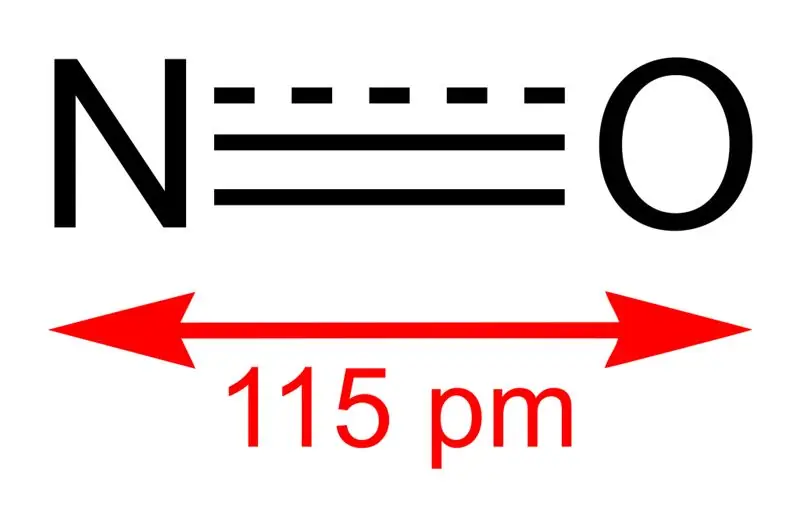
Rajah 01: Struktur Nitrogen Monoksida dan Panjang Ikatan antara N dan O
Jisim molar sebatian ini ialah 30 g/mol. Ia berlaku sebagai gas tidak berwarna. Di samping itu, takat leburnya ialah −164 °C manakala takat didih ialah −152 °C, yang merupakan nilai yang sangat kecil jika dibandingkan dengan oksida nitrogen yang lain. Kita boleh menghasilkan radikal bebas ini melalui pengoksidaan ammonia pada 850 °C dengan kehadiran pemangkin platinum. Walau bagaimanapun, pada skala makmal, kita boleh menyediakannya dengan mengurangkan asid nitrik cair dengan kuprum.
Apakah itu Dinitrogen Pentoxide?
Dinitrogen pentoksida ialah sebatian tak organik yang mempunyai formula kimia N2O5 Kami memanggilnya nitrogen pentoksida. Ia adalah nitrogen oksida binari. Selain itu, ia tidak stabil dan boleh bertindak sebagai pengoksida yang berbahaya. Jisim molar sebatian ialah 108.01 g/mol. Ia wujud padat warna putih.
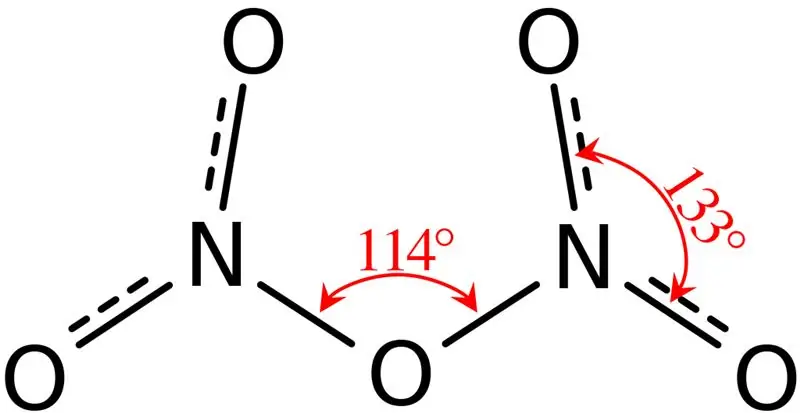
Rajah 02: Struktur Dinitrogen Pentoksida
Tambahan pula, takat lebur sebatian ini ialah 41 °C dan, pada 47 °C sebatian ini mengalami pemejalwapan. Sebatian ini bertindak balas dengan air, memberikan asid nitrik. Selain itu, bentuk molekul molekul dinitrogen pentoksida adalah planar. Kita boleh menghasilkan sebatian ini melalui dehidrasi asid nitrik dengan fosforus pentoksida.
Apakah Perbezaan Antara Nitrogen Monoksida dan Dinitrogen Pentoksida?
Nitrogen monoksida ialah sebatian tak organik yang mempunyai formula kimia NO manakala Dinitrogen pentoksida ialah sebatian tak organik yang mempunyai formula kimia N2O5 Perbezaan utama antara nitrogen monoksida dan dinitrogen pentoksida ialah nitrogen monoksida ialah gas tidak berwarna manakala dinitrogen pentoksida ialah pepejal putih. Selain itu, kita boleh menghasilkan nitrogen monoksida melalui pengoksidaan ammonia pada 850 °C dengan kehadiran pemangkin platinum. Walau bagaimanapun, penghasilan dinitrogen pentoksida adalah melalui dehidrasi asid nitrik dengan fosforus pentoksida. Apabila mempertimbangkan bentuk molekul, nitrogen monoksida adalah linear manakala dinitrogen pentoksida adalah planar.
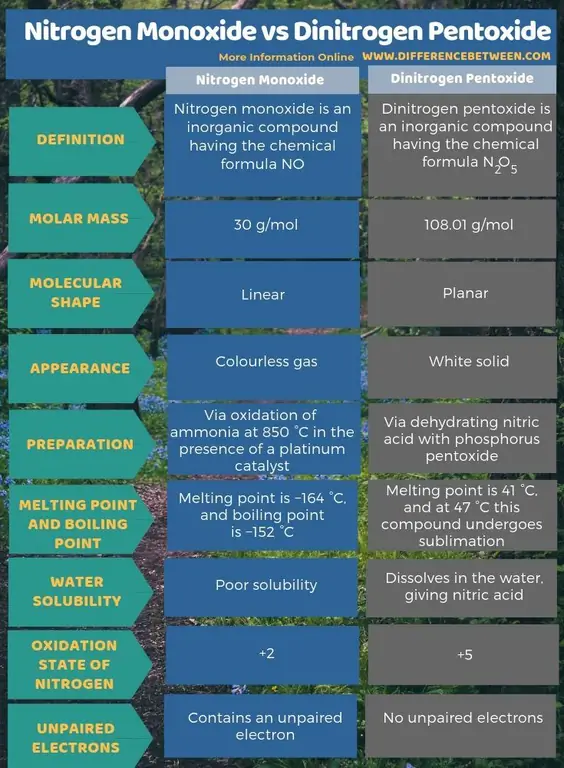
Ringkasan - Nitrogen Monoksida lwn Dinitrogen Pentoxide
Nitrogen monoksida ialah sebatian tak organik yang mempunyai formula kimia NO manakala Dinitrogen pentoksida ialah sebatian tak organik yang mempunyai formula kimia N2O5 Perbezaan utama antara nitrogen monoksida dan dinitrogen pentoksida ialah nitrogen monoksida ialah gas tidak berwarna manakala dinitrogen pentoksida ialah pepejal putih.






